Akciós potenciál
Ahogy akciós potenciál , rövidített AP , van a fiziológiája átmeneti eltérés a jellemző membránpotenciál egy sejt a maradék potenciál , ill. Az akciós potenciál automatikusan kialakul a sejtre jellemző görbével a sejt gerjesztésére (gerjesztésére), és elektromos jelként terjed a sejtmembránon keresztül . Köznyelven az idegsejtek akciós potenciáljait „idegimpulzusoknak” is nevezik.
Csak ingerelhető sejtek generálhatnak akciós potenciált az ingerekre vagy jelekre reagálva, a membrán vezetőképességének rövid távú változásain keresztül, amelyek a membránjukban lévő speciális feszültség által vezérelt ioncsatornák közötti kölcsönhatások eredményeként alakulnak ki . Időfüggő aktivációjuk különböző ionáramokhoz vezet, ennek megfelelően eltolódott potenciálkülönbségekkel. Ennek eredményeként olyan akciós potenciál alakul ki, amelyben a repolarizáció fázisa követi a depolarizáció fázisát egy lehetséges fennsík után poszt-oszcilláló hiperpolarizációval . Ez a folyamat tipikus formában automatikusan zajlik, amikor egy bizonyos küszöbpotenciál elérhetőtúllépve, és csak egy bizonyos refrakter időtartam után aktiválható újra.
Az állatokban az ingerlõ sejtek nemcsak idegsejteket, hanem izomsejteket és néhány szekréciós sejtet is tartalmaznak. Az idegsejtek ingereket vagy jeleket kapnak más sejtektől, átalakítják azokat membránpotenciál-változásokká, és akciós potenciálokat (stimulációképződést) alakíthatnak ki, mint egy sejt saját jelét, amelyet az axon mentén egy idegrostban továbbítanak (→ gerjesztési vezetés ), és továbbítanak más sejtekbe. szinapszisokon keresztül (→ gerjesztés átvitel ). Izomsejteket elérte keresztül a neuromuszkuláris szinapszisokban , ami szintén izgatott, majd formában akciós potenciálok, amely által vezérelve membrán kiemelkedések, mert a izomrostok szerződés . Gland sejteket elérte keresztül neuroglandular szinapszisok ; speciális neuroendokrin sejtek képezhetnek akciós potenciált, amelyet neurohormonok felszabadulása követ.
Ezen túlmenően, akciós potenciálok is előfordulnak egyedi sejtek - például Paramecia és diatómák -, valamint a többsejtű algák ( csillár algák ), vaszkuláris növények ( mimóza ) és gombák .
történelem
A bolognai Luigi Aloisio Galvani felfedezte az izommozgások jelenségét az elektromos erők következtében , a boncolt békák combjának megrángásaként. 1791-ben közzétett, az idegekben és az izmokban található „állati elektromos folyadékról” tett megállapításai arra késztették Alessandro Voltát, hogy vizsgálja meg a galvanizmust , amelynek eredményeként 1799-ben feltalálták az első elemet - Voltaic oszlopnak hívták . A Volta ezt a közvetlen feszültségnek az élőlényekre gyakorolt hatásainak tanulmányozására is felhasználta .
Alan Lloyd Hodgkin és Andrew Fielding Huxley 1952-ben bemutatott egy matematikai modellt, amely a tintahal óriási axonjában az akciós potenciál kialakulását magyarázza a különféle ioncsatornák egymásra hatása révén, és amely Hodgkin-Huxley modell néven vált híressé. Erre a felfedezésre a két kutató John Ecclesszel együtt 1963-ban megkapta az orvosi Nobel-díjat .
Alapok
A cselekvési potenciál a sejttípusra jellemző formában fut. Idegsejteknél ez gyakran csak körülbelül egy-két milliszekundumot vesz igénybe, a vázizomsejtek alig hosszabbak, a szívizomsejtek általában 200 ms felett vannak. Az ingertől függően nincsenek erősebb vagy gyengébb cselekvési potenciálok, inkább válaszok mindenre vagy semmire . A jelerősség tehát az akciós potenciálok gyakoriságából adódik. Az idegsejtek, azok jellemzően akkor keletkeznek az axon hegyen , és továbbítják a sorozat mentén az axon . Az akciós potenciálok is visszafelé terjedhetnek a sejttesten és a dendriteken; ennek a továbbításnak a funkcióját még vizsgálják. Az axonok terjedt sejttesten a terminál gomb van az úgynevezett orthodrom , ellenkező hívják ellenirányú .
Az akciós potenciál kialakulásának előfeltétele a sejt plazmamembránjának különleges tulajdonságai . Az ioncsatornák különböző csoportjaival rendelkező speciális berendezés a pályaforma jellemzőiben tükröződik. Felkelés akkor következik be, amikor a membránpotenciál elmozdul a nyugalmi értéktől és elmozdul a kevésbé negatív értékek irányába. Ha ez a kezdeti pre-depolarizáció elér egy bizonyos küszöbértéket, akkor aktiválódnak az úgynevezett küszöbpotenciál (kb. -55 mV), feszültség által vezérelt ioncsatornák , amelyek láncos sorrendben nyílnak meg az ionáramok engedélyezéséhez, majd ismét deaktiválják azokat.
A csatornák ezen nyitási és zárási folyamatainak láncolata során a membrán vezetőképessége a különböző ionok számára ideiglenesen megváltozik. A kapcsolódó rövid távú ionáramok együttesen egy jellegzetes potenciálgörbéhez vezetnek. Alakja a sejthez viszonyítva azonos, függetlenül a kiváltó küszöböt meghaladó inger erősségétől. A potenciál rövid távú változásai most (elektrotonikusan) átterjednek a szomszédos membrán területére, és ezután ismét az akciós potenciálhoz vezethetnek, amely a gerjesztés vezetésének alapja.
Potenciális görbe

A nyugalmi membránpotenciál alapján, amely az idegsejtekben a sejttípustól függően −90 és −70 mV között van, az akciós potenciál négy fázisát különböztetjük meg:
- Az iniciációs fázisban egy inger a negatív feszültséget nulla felé tereli ( depolarizáció ). Ez lassan vagy gyorsan megtehető, és a küszöbérték alatt visszafordítható. Ilyen inger lehet térben megközelítő akciós potenciál vagy posztszinaptikus ionáram.
- A küszöbpotenciál túllépése esetén a depolarizáció hirtelen felgyorsul ( felütés ). A membránpotenciál még pozitívvá is válik ( túllövés ).
- A +20 és +30 mV közötti maximumot a nyugalmi potenciál felé való visszatérés követi ( repolarizáció ).
- Számos idegsejtben a nyugalmi potenciál kezdetben alulmarad z-ig. B. −90 mV, és végül alacsonyabb negatív értékekből ismét elért. Ezt hiperpolarizációnak vagy hiperpolarizáló posztpotenciálnak nevezik . A hiperpolarizáció során további akciós potenciál nem váltható ki.
Az akciós potenciál időbeli lefutása néhány száz milliszekundumot meghaladhat , például a szívizomsejtekben. Az idegsejtek esetében viszont egy akciós potenciál csak kb. 1-2 ms. Ezután kiváltható egy másik cselekvési potenciál, bár nem azonnal, de csak egy bizonyos idő elteltével. A sejt már ebben az úgynevezett refrakter fázisban van a repolarizáció során, amíg ugyanazon körülmények között ismét képes akciópotenciált képezni.
Itt megkülönböztetünk abszolút refrakter időt (kb. 0,5 ms az idegsejtek esetében), amelyben egyáltalán nem lehet kiváltani akciós potenciált, és a relatív refrakter időt (kb. 3,5 ms idegsejtek esetén), amelyben erősebb ingerekre van szükség a megnövekedett küszöb potenciális vagy csak torz potenciál görbe váltja. Az a maximális frekvencia, amellyel az idegsejt képes akciós potenciálokat kialakítani és szignálként sorozatban továbbítani, a refrakter periódusoktól függ.
okoz
Az akciós potenciál megértéséhez meg kell érteni az egyes ionok egyensúlyi potenciálját, amint azt a membránpotenciál cikkben leírjuk . Ez a feszültség a külső / belső koncentrációs aránytól függ, és a Nernst-egyenlet segítségével kiszámítható . Ha csak káliumcsatornák vannak nyitva, akkor a kálium Nernst-potenciálja (−90 mV) létrejön, ha csak nátriumcsatornák vannak nyitva, akkor a nátrium Nernst-potenciálja (+60 mV).
Ha a membrán mind a káliumot, mind a nátriumot átjárja, akkor azt a feszültséget állítjuk be, amelynél a két áram összege nulla. A membránpotenciál közelebb van egy ion Nernst-potenciáljához, annál nagyobb a membrán permeabilitása ehhez az ionhoz; mennyiségileg ezt írja le a Goldman-egyenlet . A nyugalmi membránpotenciálnál elsősorban a káliumcsatornák vannak nyitva, ez magyarázza a −70 mV körüli alacsony feszültséget. Az akciós potenciál során viszont röviden túlsúlyban van a nátrium permeabilitása. Az akciós potenciál során felmerülő összes potenciál az adott időpontban fennálló permeabilitásokból származik.
Az akciós potenciál során fellépő áramok olyan kicsiek, hogy nem változtatják meg jelentősen a membrán mindkét oldalán lévő koncentrációkat. Annak érdekében, hogy a koncentrációarányok hosszú távon állandóak maradjanak, szükség van a nátrium-kálium szivattyú munkájára , amely bár ATP-t fogyaszt , három kálium-ion cserébe három nátrium-iont távolít el a sejtből.
Az ioncsatornák tulajdonságai
A nyugalmi membránpotenciálról szóló cikkben leírtak szerint a sejtek számos ioncsatornával rendelkeznek. Bizonyos, a nátrium- vagy káliumionokra specifikus ioncsatornák felelősek elsősorban az állati cselekvési potenciálért . Ezek a csatornák a membránpotenciál függvényében nyílnak, ezért feszültség-aktiváltak . A membránpotenciál nyugalmi állapotban negatív.
Például egy feszültségfüggő nátriumcsatorna (Na v- csatorna) (tulajdonságánál fogva gyorsnátrium- csatornának is nevezik ) a nyugalmi membránpotenciálnál zárva van és aktiválódik . Csatorna-specifikus érték feletti depolarizáció esetén változás következik be a transzmembrán fehérjék konformációjában. Ez a csatornát átjárhatóvá teszi az ionok számára, és megváltozik a nyitott állapot . A csatorna azonban a folyamatos depolarizáció ellenére sem marad nyitva, a membránpotenciáltól függetlenül néhány milliszekundumon belül ismét bezáródik. Ez általában a citoplazmában található csatornafehérje egy részén, az inaktivációs doménen keresztül történik, amely olyan, mint egy "dugó" a csatornában, és eltömíti azt. Ezt az állapotot zártnak és inaktiváltnak nevezzük .
Az ezt követő átmenet zárt és aktiválható állapotba csak hiperpolarizáció (vagy teljes repolarizáció esetén a szívizomsejtek esetén) lehetséges. A csatorna eleinte zárva marad , repolarizáció vagy hiperpolarizáció után aktiválható, és csak ezután nyitható meg depolarizációval. Megnyitás után a csatorna csak rövid ideig marad nyitva, mivel gyorsan zárt formára vált és inaktiválódik. Azonban, egy átmenet inaktivált , hogy nyitott nem lehetséges a depolarizált membránnal.
Nem minden csatorna nyílik egyidejűleg a membránpotenciál azonos értékén. Inkább a csatorna bizonyos állapotba való átmenetének valószínűsége feszültségfüggő. A pusztán statisztikai eloszlás olyan egyensúlyt eredményez, hogy összesen több csatorna felel meg a fent leírt modellnek.
Az egyik állapotról a másikra való áttéréshez szükséges idő szintén csatornspecifikus. A nátrium csatorna leírt, a konformációs változás zárva a nyitott vesz kevesebb, mint egy ezredmásodperc, míg a kálium-csatorna veszi körül 10 ms erre.
A feszültségen kívül számos más, gyakran kémiai tényező okozza a csatornák kinyitását vagy bezárását. Közülük csak kettőnek van bizonyos jelentősége a cselekvési potenciál szempontjából (lásd alább). Egyrészt a befelé kiegyenlítő káliumcsatornák (K ir ) önmagában nem szabályozhatók. Vannak azonban alacsony molekulatömegű, pozitív töltésű anyagok, mint például a spermium , amelyek megfelelő depolarizáció esetén eltömíthetik a csatorna pórusait (csatorna blokk, pórus blokk). Egy másik mechanizmus a káliumcsatornákat érinti, amelyek akkor nyílnak meg, amikor a kalciumionok intracellulárisan kötődnek hozzájuk (általában nagyon alacsony koncentrációban intracellulárisan).
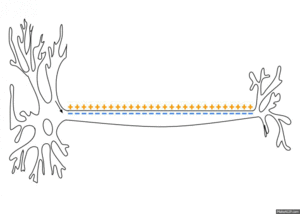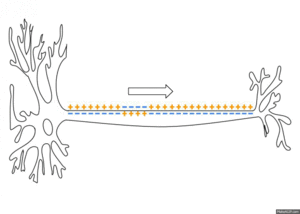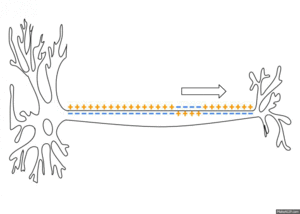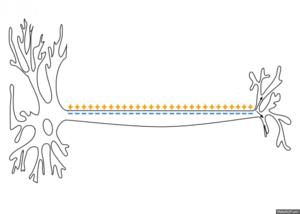
eljárás

Kezdő pozíció
A kiindulási helyzetben a sejt nyugalomban van, és megmutatja nyugalmi membránpotenciálját. Szinte az összes nátriumcsatorna zárva van, csak bizonyos káliumcsatornák vannak nyitva. A káliumionok lényegében meghatározzák a nyugalmi membránpotenciált. Az összes ionmozgás irányát és erősségét az adott ionok elektrokémiai hajtóereje határozza meg . Mindenekelőtt a nátriumionok gyorsan beáramlanak a sejtbe, amint a csatornák megnyílnak számára az uralkodó koncentrációs gradiens miatt .
Kezdeményezési szakasz
Az iniciációs fázis során a membránpotenciál oly módon változik meg, hogy az eltérjen a nyugalmi potenciáltól a csökkenő nagyságú negatív értékek irányában, amíg a töltési gradiens csökkenése el nem ér egy bizonyos küszöbpotenciált. Ez az elődepolarizáció történhet a kísérletben ingerelektród alkalmazásával, az axonhalmon a posztszinaptikus ioncsatornák (Na + , Ca 2+ ) nyílásán keresztül , vagy az axonmembránon egy szomszédos elektrotonikusan átvitt (akció) potenciálon keresztül. membrán régió.
Ilyen predepolarizáló változásokkal a membránpotenciálban, például −70 és −60 mV között és azon túl, a K ir csatornákat pórusblokkolók , például spermin blokkolhatják. Ez csillapítja a káliumáramot, amelynek javító hatása van a nyugalmi potenciál irányába. Ez megkönnyíti a küszöbpotenciál elérését, és felgyorsítja a későbbi depolarizációt, amikor a nátriumcsatornák megnyílnak.
Terjesztés és túllépés
Körülbelül −55 mV feszültségnél a Na V -feszültség által vezérelt nátriumcsatornák nyitott állapotba kezdenek változni . A nátriumionok, amelyek magas külső koncentrációjuk miatt távol állnak az elektrokémiai egyensúlyuktól, beáramlanak és depolarizálják a sejtet. Ez további feszültségérzékeny csatornákat nyit, és még több ion áramolhat be: A gyors felütés túllépéshez vezet (polarizáció / töltés megfordulás). A küszöbpotenciál túllépése után a „robbanásveszélyes” depolarizációt tehát pozitív visszacsatolás okozza .
Repolarizáció
Még mielőtt a maximális potenciál elérné a túllövést, a Na V csatornák inaktiválódni kezdenek . Ugyanakkor a K V feszültségfüggő káliumcsatornái játszanak szerepet, a cellából K + ionok áramlanak ki. Bár ezen ioncsatornák küszöbértéke hasonló értékeken van, sokkal hosszabb ideig tart nyitni. A Na vezetőképességének maximuma alatt ezek a káliumcsatornák csak félig vannak nyitva; akkor érik el a maximumot, amikor szinte az összes Na-csatorna inaktiválva van. Ezért a Na vezetőképességi maximum kissé megelőzi a túlfeszültség maximumait, de a K vezetőképességi maximum a legmeredekebb repolarizáció fázisában van.
A repolarizáció során a potenciál ismét megközelíti a nyugalmi potenciált. A K V csatornák bezáródnak, és a K ir pórustömbje megszakad, ami fontos a nyugalmi potenciál stabilizálása szempontjából. A Na V csatornák lassan újra aktiválhatók. A repolarizációt néha hiperpolarizációnak is nevezik, amikor ezt a kifejezést a membránpotenciál növekvő negatívumaként határozzák meg.
Post hiperpolarizáció
Sok sejtben, különösen az idegsejtekben, még mindig megfigyelhető a nyugalmi potenciált meghaladó hiperpolarizáció . Ez egy további megnövekedett kálium-vezetőképességgel magyarázható, ahol a potenciál még közelebb van a kálium- egyensúlyi potenciálhoz . A K-vezetőképesség megnő, mert az akciós potenciál során beáramló kalciumionok itt speciális káliumcsatornákat nyitnak meg; csak akkor normalizálódik, amikor az intracelluláris kalciumszint ismét csökken. Ha a repolarizációt már hiperpolarizációnak nevezték, akkor ezt a további süllyesztési folyamatot hiperpolarizációnak nevezik.
Tűzálló időszak
Miután az akciós potenciál alábbhagyott, egy sejt nem izgatható rövid ideig . A szív szívizomsejtjeiben ez a fázis - amelyet itt "platófázisnak" is neveznek - különösen tartós, amelyet "lassú kalcium beáramlásnak" tulajdonítanak. Ez a tény azért fontos, mert megakadályozza a gerjesztés retrográd visszatérését (egyirányúság). Ennek az időtartamnak, a refrakter periódusnak az időtartama a Na V- csatornák reaktivációjának időbeli lefolyásától függ . Az abszolút tűzálló szakaszban röviddel a túllövés után, amikor a repolarizáció még folyamatban van, ezek a csatornák egyáltalán nem nyithatók meg. Azt is mondják, hogy a küszöb végtelen. A relatív refrakter szakaszban erősebb ingerekre van szükség, és gyengébb akciós potenciálokat kapunk. Itt a küszöbérték a végtelentől a normálértékig mozog.
Küszöbpotenciál
Az akciós potenciál kiváltását általában egy bizonyos küszöbpotenciál túllépéseként írják le, amelyből a nátriumcsatornák együttesen nyílnak meg. Annak ellenére, hogy igyekeztünk ilyen pontos „tűzküszöböt” találni, nem lehet fix feszültségértéket meghatározni az akciós potenciál feltételeként. Ehelyett az idegsejtek a membránfeszültségeket kiváltó, viszonylag széles sávra lőnek. Ezért az idegtudomány tartózkodik a küszöbpotenciál fix értékének gondolatától. A rendszerelmélet szempontjából a cselekvési potenciál létrehozásának folyamatát a kettéágazással lehet legjobban leírni , mint például a Hodgkin-Huxley modell esetében . Mindazonáltal, a szakirodalomban is gyakran előfordul, hogy továbbra is küszöbről beszélnek a „nyugalom és a cselekvési potenciál közötti szürke terület” körülhatárolása érdekében.
Állati cselekvési potenciálok
A Purkinje sejtekben az akciós potenciál frekvenciája nemcsak feszültség által aktivált nátriumcsatornákkal, hanem feszültség által aktivált kalcium csatornákkal is módosítható.
Növényi akciós potenciálok
Elvileg a növények és gombák sejtjei elektromos úton is gerjeszthetők. Az állati akciós potenciál fő különbsége az, hogy a depolarizációt nem a (pozitív töltésű) nátriumionok beáramlása okozza, hanem a (negatív töltésű) kloridionok kiáramlása . A (pozitív töltésű) káliumionok későbbi szökésével együtt - amely repolarizációt okoz mind az állati, mind a növényi sejtekben - ez a kálium-klorid ozmotikus veszteségét jelenti a növényi sejtek számára ; másrészt az állat akciópotenciálja ozmotikusan semleges az egyenlő mennyiségű nátrium beáramlás és kálium kiáramlás miatt.
Az elektromos és ozmotikus események összekapcsolása a növényi akciós potenciálban arra utal, hogy az állati és növényi sejtek közös egysejtű őseiben az elektromos ingerelhetőség a só egyensúlyának szabályozását szolgálta változó sótartalmú körülmények között , míg az állatok többsejtű organizmusok ozmotikusan semleges jelátvitele szinte az állandó sótartalom evolúciós szempontból fiatalabb eredményt képvisel. Ennek megfelelően egyes vaszkuláris növények (például a Mimosa pudica ) akciópotenciálainak jelző funkciója függetlenül fejlődött az állati sejtek működésétől.
irodalom
- Stefan Silbernagl, Agamemnon Despopoulos: A fiziológia zseb atlasza. 6. kiadás. Thieme Publishing Group, Stuttgart 2003, ISBN 3-13-567706-0 .
web Linkek
- Akció potenciális továbbítás - Flash animáció 4 szakaszban az informatik.uni-ulm.de oldalon
Egyéni bizonyíték
- ^ H. Machemer, A. Ogura: A membránok ionos vezetőképessége a csillós és a decilizált Parameciumban. In: A Journal of Physiology . szalag 296 , 1979, pp. 49-60 , PMID 529.122 .
- ^ AR Taylor: Gyors Na + / Ca2 + -alapú akciós potenciál egy tengeri kova esetében . In: PLOS ONE . szalag 4. cikk (3) , 2009, e4966 . Cikk , PMID 19305505 .
- ↑ a b M. J. Beilby: Akciópotenciálok a charophytákban . In: Int. Rev. Cytol. szalag 257. , 2007, pp. 43-82 , doi : 10.1016 / S0074-7696 (07) 57002-6 , PMID 17280895 .
- S T. Sibaoka: Izgalmas sejtek a Mimosa-ban . In: Tudomány . szalag 137 , 1962, pp. 226 , PMID 13912476 .
- ^ A b C. L. Slayman, WS Long, D. Gradmann: Akciópotenciálok a Neurospora crassa , egy micélium gomba . In: Biochimica et biophysica acta . szalag 426 , 1976, pp. 737-744 , PMID 130926 .
- ↑ a b L. A. Galvani: De viribus electricitatis in motu musculari. ("Az elektromosság erőiről az izommozgásokban"). Bologna 1791. (online)
- ↑ M. Piccolino: Luigi Galvani és az állati elektromosság: két évszázaddal az elektrofiziológia megalapozása után . In: Az idegtudomány trendjei . szalag 20 , no. 10 , 1997, pp. 443-448 , doi : 10.1016 / S0166-2236 (97) 01101-6 .
- Pic M. Piccolino: A Voltaic-akkumulátor (1800–2000) kétszázadik évfordulója: a mesterséges elektromos szerv . In: Az idegtudomány trendjei . szalag 23 , no. 4 , 2000, pp. 147-151 , doi : 10.1016 / S0166-2236 (99) 01544-1 .
- ↑ AL Hodgkin, AF Huxley: A membrán áramának kvantitatív leírása és alkalmazása az ideg vezetésében és gerjesztésében . In: J. Physiol. szalag 117 , 1952, pp. 500-544 , PMID 12991237 .
- ↑ John PJ Pinel, Pauli Pauli : Biopsychologie. 6., frissítés Kiadás. Pearson Studium, 2007, ISBN 978-3-8273-7217-8 , 110. o.
- ↑ Robert F. Schmidt : Az emberek élettana: Patofiziológiával. Springer Verlag, 2007, ISBN 978-3-540-32908-4 , 88. o.
- ↑ E. Hosy, C. Piochon, E. Teuling, L. Rinaldo, C. Hansel: SK2 csatorna expressziója és működése a kisagyi Purkinje sejtekben. In: A Journal of Physiology. 589. évfolyam, 2011. július 14., Pt. 3433–3440, ISSN 1469–7793 . doi: 10.1113 / jphysiol.2011.205823 . PMID 21521760 . PMC 3167108 (ingyenes teljes szöveg).
- Zh N. Zheng, IM Raman: Szinaptikus gátlás, gerjesztés és plaszticitás a kisagyi sejtek idegsejtjeiben. In: Cerebellum. 9. évfolyam , 1. szám, 2010. március, 56-66. Oldal, ISSN 1473-4230 . doi: 10.1007 / s12311-009-0140-6 . PMID 19847585 . PMC 2841711 (ingyenes teljes szöveg).
- ↑ H. Mummert, D. Gradmann: Az akciós potenciálokat a Acetabularia : mérés és szimuláció a feszültségfüggő fluxus . In: Journal of Membrane Biology . szalag 124 , 1991, pp. 265-273 , PMID 1664861 .
- ↑ D. Gradmann: modellek rezgések a növényekben . In: Austr. J. Plant Physiol. szalag 28. , 2001, p. 577-590 .
- ^ D. Gradmann, J. Hoffstadt: Iontranszporterek elektrocsatolása növényekben: Interakció belső ionkoncentrációkkal . In: Journal of Membrane Biology . szalag 166 , 1998, pp. 51-59 , PMID 9784585 .
- ↑ D. Gradmann, H. Mummert: Plant akciós potenciálok. In: RM Spanswick, WJ Lucas, J. Dainty: Plant Membrane Transport: Current Conceptual Issues. Elsevier Biomedical Press, Amsterdam 1980, ISBN 0-444-80192-8 , 333-344.