Klaszter (fizika)

C 540 óriási mérete miatt nagyon labilis gömbszerkezet, mivel csak gömb alakú . Az ilyen nagy fullerének tehát csak a C 60 , C 70 és a nagyobb fullerének , ún. "Hagymák"kapcsánstabilak.
A klaszter atomok vagy molekulák gyűjteménye, amelyek száma 3 és 10 millió között van.
Kis méretük miatt a klaszterek tulajdonságai eltérnek a makroszkopikus szilárd anyag tulajdonságaitól . Az atom- és a molekuláris fizika fogalmai gyakran kudarcot vallanak, amikor ilyen kis részecskék tulajdonságait kell megmagyarázni. A klaszterek tulajdonságai tehát kapcsolatot teremtenek egyrészt az atom- és a molekuláris fizika, másrészt a szilárdtestfizika között. A kutatás tárgya ezen a területen az, hogy miként alakulnak ki egy szilárd anyag makroszkopikus tulajdonságai az atom tulajdonságaiból vagy molekula. A felület és a térfogat atomjainak aránya meghatározó a klaszter számos tulajdonsága szempontjából.
További különbséget teszünk egy szabad és egy letétbe helyezett fürt között. Ez utóbbi egy felszínen van, míg a szabad klaszter szabadon mozog az űrben.
Osztályozás
A klasztereket általában az atomok száma ( n ) szerint osztják fel :
- n = 3–12 atom ( mikroklusterek ): A mikroklaszterek esetében a klaszter összes alkotóeleme még mindig a felszínen van . Az atom- és molekulafizika, valamint a felületi fizika fogalmai és módszerei alkalmazhatók és hasznosak.
- n = 13–100 atom ( kis klaszterek ): A kis klaszterek tulajdonságait nagyrészt kvantumhatások határozzák meg . Az elektronikus energiaszintek már elég közel vannak egymáshoz, de az atomok száma még mindig túl kicsi egy szalagszerkezethez, mint a szilárd testben. Egy további atom vagy molekula beépítése sokat változtathat. Gyakran sok izomer klaszter szerkezet létezik , szorosan elosztva egymástól az energiaszinttel. A molekuláris fogalmak elveszítik hasznosságukat. Itt is a felületi fizika továbbra is nagyon fontos szerepet játszik, mivel a klaszterben nagy a felszíni atomok és a térfogat atomok aránya.
- n = 100–1000 atom ( nagy klaszterek ): fokozatos átmenet figyelhető meg a szilárd anyag tulajdonságainál, például átmenet a kristályrácsokban ( például a króm átmenet az fcc (<490) és a bcc (> 490) között n = 490 körül ; ezeknek az értékeknek a fluktuációs tartománya 100 atom).
- n > 1000 atom ( kis részecskék vagy nanokristályok )
Néhány, de nem minden szilárd tulajdonság kialakult. Körülbelül 50 000 atomból a tulajdonságok olyan erősen fejlődtek, hogy onnantól kezdve szilárd anyagról beszélünk.
Osztályozás a kémiai kötés szerint
- fémes klaszterek : a delokalizált elektronok félteljes sávja, példák: alkálifém-klaszterek, Al , Cu , Fe , Pt , W , Hg klaszterek; mindegyik n > 200 atomnál, átlagos kötési energia: 0,5-3 eV
- kovalens klaszterek : sp hibridizációval összehangolt elektronpárokon keresztül kötődnek; Példák: C klaszterek (a legismertebb példák a fullerének , lásd még a fenti képet. A szén nanocsövek és a gyémánt klaszterek is a szén klaszterekhez tartoznak); Si , Hg klaszterek; mindegyik 30 < n <80 atomot jelent, átlagos kötési energia: 1–4 eV, Hg ≈ 0,5 eV
- Ionos klaszterek : Coulomb-erők kötődése az ionok között, példák: ( KF ) -, ( CaI 2 ) klaszterek, átlagos kötési energia: 2–4 eV
- Klaszterek hidrogénkötésekkel : erős dipól-dipól vonzás, példák: ( HF ), ( H 2 O ) klaszterek, átlagos kötési energia: 0,15-0,5 eV
- molekuláris klaszterek : Van der Waals- klaszterek, plusz gyenge kovalens komponensek, példák: (I 2 ) -, (As 4 ) -, (S 8 ) -, szerves molekuláris klaszterek, átlagos kötési energia: 0,3–1 eV
- Van der Waals-klaszter : atomok és molekulák indukált dipólus-kölcsönhatása zárt elektronikus héjjal, példák: nemesgáz , ( H 2 ), ( CO 2 ), Hg klaszterek; mindegyik n <10 atomot jelent, átlagos kötési energia: 0,001-0,3 eV
A szabad klaszterek felépítése
Friedel uralma kiemelkedő jelentőségű a szabad klaszterek szerkezete szempontjából :
- A legtöbb szomszédos kötést tartalmazó klaszterstruktúrának van a legnagyobb kötési energiája, és ezért az összes lehetséges szerkezet közül a legstabilabb.
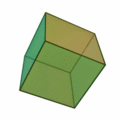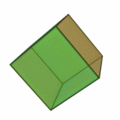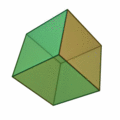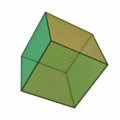
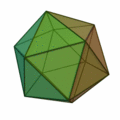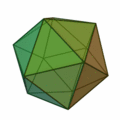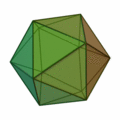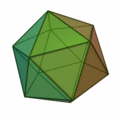
Ez a szabály általában olyan struktúrákat eredményez, amelyek a platoni szilárd anyagok mintájára épülnek :
Itt különösen fontos az ikozaéder szerkezete (a jobb szélső felépítés) , amely különösen gyakran fordul elő az n > 12 atomszámú klasztereknél . A test minden sarkában és az ikozaéder szerkezet belsejében atom található. A 12 sarok miatt 12 felületi atom és 1 térfogatú atom van egy 13 atomos klaszterhez. Nagyobb atomszám esetén az új héjat atomokkal töltik fel, így ikozaédert képeznek, ahol a k . Héjban a nagyobb kötési hosszúság miatt 10 k + 2 atomot talál a héjtérben. Tehát 12 atom van az első héj számára, pontosan 42 további hely van a második héj számára, 92 atom a harmadik héjra és így tovább. Mint a k = 1 héj esetében, ezeknek a héjaknak is van 12 atomja a sarkokban ikozaéder, és további 10 k ² - 10 atomok a felületen. Ezek a koncentrikus icosahedra ezután kell elképzelni , mint matryoshkas azokkal az atomokkal felszínükön. Csakúgy, mint az atomfizikában a stabil nemesgáz atomokkal, a héjzárások miatt is vannak nagyon stabil fürtök. A zárt klaszterhéj-szerkezet csak néhány klaszterméret esetén eredményez: n = 13, n = 55, n = 147, n = 309, n = 561, n = 923 és n = 1415; "varázsszámoknak" hívják őket. Ezeket a nagyon stabil, feltöltött atomhéjakkal rendelkező klasztereket Mackay icosahedrának hívják. A fenti ábra platóni szilárd anyagai a mikroklusterekben, a hexaéder nagyobb klaszterekben is megjelennek.
A varázsfürt számai a következő képlet segítségével számíthatók ki:
- = Az atomok teljes száma
- = Peremenként lévő atomok száma
irodalom
Bevezető irodalom
- H. Haberland: Kísérleti fizika tankönyv: Kísérleti fizika tankönyv 5. Gázok, nanorendszerek, folyadékok: gázok, nanorendszerek, folyadékok . Fejezetfürt. Szerk .: Ludwig Bergmann, Clemens Schaefer, Karl Kleinermanns. 2. kiadás. Gruyter, 2005, ISBN 3-11-017484-7 .
- Gutmann Viktor, Edwin Hengge: Szervetlen kémia. Bevezetés . 5. kiadás. Wiley-VCH, 1990, ISBN 3-527-28159-2 , fejezet klaszterek .
Fontos publikációk
- AL Mackay : Egyenlő gömbök sűrű, nem kristálytani csomagolása . In: Acta Crystallographica . szalag 15 , no. 9. , 1962, pp. 916-918 , doi : 10.1107 / S0365110X6200239X ( Mackay ikozaéder ).
- Jortner, Joshua: A klaszterek szintstruktúrája és dinamikája . In: A Bunsen Fizikai Kémia Társaság jelentése . szalag 88 , 1984, pp. 188-201 .
Egyéni bizonyíték
- ↑ Oliver Rattunde; Hellmut Haberland: Clusterphysik . Letöltve: 2017. január 19.
- ^ A b Erwin Riedel , Christoph Janiak : Szervetlen kémia . 9. kiadás. De Gruyter, Berlin 2015, ISBN 3-11-035526-4 , pp. 190 f .
- ↑ Helmut Haberland, Karl Kleinermanns, Frank Träger: Bergmann-Schaefer - Experimentalphysik 5. kötet - Gázok, nanorendszerek, folyadékok - 9. fejezet Klaszterek . szalag 5 . Walter de Gruyter, 2006, ISBN 978-3-11-017484-7 , p. 817 ff .