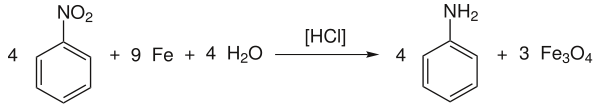anilin
| Szerkezeti képlet | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||||||||
| Tábornok | ||||||||||||||||||||||
| Vezetéknév | anilin | |||||||||||||||||||||
| más nevek |
|
|||||||||||||||||||||
| Molekuláris képlet | C 6 H 7 N | |||||||||||||||||||||
| Rövid leírás |
olajos, színtelen vagy barna folyadék |
|||||||||||||||||||||
| Külső azonosítók / adatbázisok | ||||||||||||||||||||||
| ||||||||||||||||||||||
| tulajdonságait | ||||||||||||||||||||||
| Moláris tömeg | 93,13 g mol -1 | |||||||||||||||||||||
| Fizikai állapot |
folyadék |
|||||||||||||||||||||
| sűrűség |
1,02 g cm -3 |
|||||||||||||||||||||
| Olvadáspont |
-6 ° C |
|||||||||||||||||||||
| forráspont |
184 ° C |
|||||||||||||||||||||
| Gőznyomás |
0,681 hPa (20 ° C) |
|||||||||||||||||||||
| oldhatóság |
vízben szegény (36 g l -1 a 20 ° C -on) |
|||||||||||||||||||||
| Törésmutató |
1.5863 (20 ° C) |
|||||||||||||||||||||
| biztonsági utasítások | ||||||||||||||||||||||
| ||||||||||||||||||||||
| MAK |
|
|||||||||||||||||||||
| Toxikológiai adatok | ||||||||||||||||||||||
| Amennyire lehetséges és szokásos, SI egységeket használnak. Eltérő rendelkezés hiányában a megadott adatok a szabványos feltételekre vonatkoznak . Törésmutató: Na-D vonal , 20 ° C | ||||||||||||||||||||||
Az anilin ( spanyolból vagy arabból : an-nil = kék = indigó szín ) vagy a benzolamin tiszta, színtelen vagy enyhén sárgás színű, olajos folyadék, különleges illattal, amely gyorsan vörösesbarna lesz a levegőben. Ez egy benzolgyűrű egy aminocsoport (-NH 2 ), és így egy aromás amin . Amikor keverve a savakkal , ez képezi anilin sói . A bázikus hatása anilint gyengült a mezomer hatása , mivel ez csökkenti az elektronsűrűség az aminocsoport.
elnevezéstan
A szisztematikus IUPAC név benzolamin. Azonban a most preferált IUPAC név az anilin. Az anilin származékaira történelmileg "anil" szótagot használnak; például anilazin , acetanilid .
sztori
Anilin-ben először elő 1826-ban Otto Unverdorben által desztillálásával mész a indigó . A kapott olajat kristálynak nevezte el (jellemző tulajdonsága a kristályosítható sók képződése savakkal). 1834 -ben Friedlieb Ferdinand Runge először izolált anilint a régóta legfontosabb forrásból, a kőszénkátrányból , és elnevezte kyanolnak (kék olaj, az anyag klórmész -oldattal szembeni viselkedése alapján). Carl Julius Fritzsche 1840 -ben kapta az anilint az antranilsav lepárlásából, és bizonyítani tudta a Zinin termék azonosságát . Zinin anilint (amelyet benzidamnak nevezett ) nitrobenzolból nyert hidrogén -szulfiddal redukálva. AW Hofmann kimutatta, hogy ezek a vegyületek azonosak; a nitrobenzolt anilinné is képes redukálni egy jelentősen javított eljárással (cink + sav).
Az anilint a Badische Anilin- und Soda-Fabrik ( BASF ) 1897 óta használja az indigó festék előállítására, amelyet korábban csak növényi alapanyagokból ( Heumann-szintézis ) nyertek . Az anilin már elő nagy mennyiségben előre, például Agfa ( Actien-Gesellschaft für Anilin-Fabrication ) 1873-től kezdődően. A jól ismert használata a festéket anilin bőr . Az anilint a nyomtatási technológiában is használták, többek között: aki még ma is használta a flexo becenevén flexográfiai nevet, mivel csak az anilin jó nyomtatási minőségével lehetett előállítani.
Gyártás
Iparilag előállított anilin nitrobenzol hidrogénezésével a gázfázisban 270 ° C -on és 1,25 bar nyomáson réz katalizátoron , szilícium -dioxidon. Ehhez fluid ágyas reaktorokat használnak.
Ezenkívül a hidrogénezés lehetséges nikkel -szulfid katalizátoron , alumínium -oxidon , rögzített ágyas reaktorban.
Az a folyamat, melynek során az anilint kaptunk csökkentésével nitrobenzolt vas jelenlétében sósavat ( Béchamp csökkentés ) elavult:
Ezután égetetlen mésszel (CaO) semlegesítik , és az anilint vízzel együtt ledesztillálják. A melléktermékként képződött vas (II, III) -oxid felhasználható pigmentként .
Vannak más folyamatok, például az ammonolízis a klór-benzol , vagy fenol :
használat
A vegyiparban elsősorban nyersanyagként használják a színek és szintetikus szálak szintéziséhez, de szintetikus gumi és gyógyszerek előállításához, valamint az űrutazásban a hipergolikus üzemanyagok összetevőjeként is .
Reakciók
Az anilin gyenge bázis . Az aromás aminok, mint az anilin, általában sokkal gyengébb bázisok, mint az alifás aminok.
Az anilin gyenge lúgosságát az elektronegatívabb sp 2 szén indukciós hatásának és a rezonanciahatások kombinációjának tulajdoníthatjuk , mivel a nitrogén magányos pár részlegesen delokalizálódik a benzolgyűrű π rendszerébe.
Ez azonban nem veszi figyelembe a szolvatációt, amely lényegében meghatározza az anilin alaposságát. Az ammónia vonatkozásában például az anilin gázfázisa bázikusabb, míg a vizes oldat 10 000 -szer kevésbé bázikus.
Az aminocsoportnál
Az anilin a legegyszerűbb aromás amin, és csak kevéssé oldódik vízben. Savat (például sósavat) adnak az anilinhez, hogy elősegítsék vagy növeljék a vízben való oldhatóságot; ez azonnali sóképződéshez vezet. A hidroklorid -anilinium-kloridot képződik sósavval :
Ha az anilint hagyjuk reagálni sójával (például anilin -hidrokloriddal ) a melegben, akkor difenilamin képződik :
Az anilin és ecetsavanhidriddel eredményez N -fenil-acetamid ( acetanilid ):
A nitrobenzol anilinből történő előállítása is lehetséges. Az anilint nitrogén -benzollá alakítják át a köztes fázisú nitrozobenzolon keresztül oxidálószerrel (például hidrogén -peroxid , mCPBA , kálium -permanganát , króm (VI) -oxid vagy ólom (IV) -oxid ) .
A reakciót a nitrozo-benzol és az anilin vezet azobenzol által vízlehasító :
Közvetlen nitrálási a nitrálósav vezet oxidációja az aminocsoport. A kívánt nitroanilineket acetanilidként csak az aminocsoport előzetes védelme után kapjuk meg.
Ha csökkenti a nitroanilin most kaptunk a segítségével egy redukálószerrel (mint például cink- sósavban, nátrium-bór-hidrid , lítium-alumínium-hidrid vagy nátrium-szulfitot ), akkor kap a feniléndiaminok :
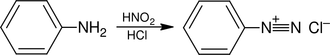
A diazotizálás néven ismert reakció is ismert. Az anilin reakcióba lép nátrium -nitrittel , például sósav vagy salétromsav jelenlétében , így benzol -diazónium -klorid keletkezik:
A benzol egy erős, instabil elektrofil a festék kémiai egy nagyszerű alkalmazás. A benzol -diazónium -klorid például vízzel reagálva fenolt képezhet nitrogénveszteséggel. A Sandmeyer-reakció jelenlétében réz (I) -klorid és sósav a hőközléssel is lehetséges - a klór-benzol is képződik egy nitrogén veszteséget. A két nitrogénatom megtartása mellett a benzol -diazónium -ion fenil -hidrazinná redukálható, például nátrium -szulfit vizes oldatában :
Ha a benzol-diazónium-kloridot hagyjuk reagálni, például lúgos 2-naftol- oldattal ( ), akkor az úgynevezett Szudán I-t kapjuk . Ezt a reakciót kapcsolási reakciónak is nevezik, pontosabban azo -kapcsolásnak :
A naftolokon kívül más kapcsoló reagensek is használhatók, például 1-naftil-amin . A lehetséges kapcsoló reagensek nagy száma miatt sok fontos azoszínezék létezik, ezért számukban a legerősebb festékosztályt alkotják.
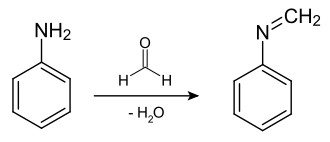
Ha az anilint az iminképződés mechanizmusának megfelelően hagyjuk reagálni a formaldehiddel (37%), akkor N -metilidén -anilint kapunk :
Először is, az anilin aminocsoportjának nitrogénje megtámadja a formaldehid aldehidcsoportját ( karbonilcsoportja ) . Az aldehidcsoport kettős kötésű oxigénje egyetlen kötéssé válik, negatív töltéssel. A nitrogén kezdetben pozitív töltésű, amíg el nem adja protonját az aldehidcsoport negatív töltésű oxigénjének. Spontán módon vagy dehidratálószer hozzáadásával a molekula ( a korábbi formaldehid hidroxilcsoportja és a nitrogén protonja) vizet leválaszt . Létrejön az R ' - N = CH - R' 'általános szerkezetű vegyület. Az N -metilidén -anilin a vegyületek azometin -osztályába (Schiff -bázisok) tartozik, és a metilidén -csoport miatt nagyon reakcióképes támadási pontja van a nukleofileknek.
Az anilin és a benzaldehid reakciója benzalanilinhez (benzilidén -anilin ) vezet :
A gyűrűn
A szulfonálási egy elektrofil aromás szubsztitúciós S E . A kén -trioxidot (SO 3 ) elektrofil részecskeként vezetik be, amely a kénsav önmagával való reakciója során keletkezik:
Az elektrofil ( kén -trioxid ) képződése :
Az elektrofil szubsztitúció ( szulfonálás ) elve szerint a szulfanilsav szintetizálható.
További elektrofil szubsztitúciók is lehetségesek. Például halogénezés , Friedel-Crafts alkilezés és Friedel-Crafts acilezés .
Az anilin katalitikus hidrogénezése katalizátor jelenlétében ciklohexil -aminhoz ( CHA ) vezet . A katalitikus hidrogénezéshez használt katalizátor általában (nemes) fémek , például palládium :
biztonsági utasítások
Az anilin erős vérméreg. Oxidálódik a vörös vér pigment hemoglobin a methemoglobin és így megakadályozza, hogy a közlekedési oxigén a vérben. A méreg lenyelés, belégzés és a bőrön keresztül felszívódhat. Enyhe mérgezés esetén a bőr és a körmök kék színűek ( cianózis ), szédülés és izgalom. Nagyobb koncentrációban fejfájás, szédülés, tudatzavar és légszomj jelentkezik. Ez utóbbi halált okozhat. A mérgezés hosszú távú tünetei gyengeségben, étvágytalanságban és hólyagrákban jelentkeznek.
1981 -ben az anilin volt az egyik oka annak a tömeges mérgezésnek is , amely Spanyolországban a szennyezett repceolaj ( spanyol olajos szindróma ) révén történt : az ipari célokra anilinnel denaturált repceolajat újra desztillálták , majd "olívaolajként" értékesítették az utcai árusokon keresztül. 20 000 ember megbetegedett, és több mint 300 meghalt. A mérgezés pontos hátterét még nem tisztázták.
Lásd még
irodalom
- Karl Aloys Schenzinger : Anilin - festékregény . 1936.
- Christian Mähr : Az alkoholtól a cukorig - tizenkét anyag, amely megváltoztatta a világot . Köln 2010, ISBN 978-3-8321-9549-6 .
- Margarete Bruns: Az azuritról, indigóról és anilinről. A kék szín történetéről. In: Emil Ernst Ploß: Régi színek könyve. A textilszínek technológiája a középkorban, a szilárd színek szemléletével. 6. kiadás. München 1989, ISBN 978-3-89164-060-9 , 14-20.
- "Hozzájárulás a tudományos felfedezések történetéhez" - Friedlieb Ferdinand Runge anilin felfedezése . In: A pavilon . 4. kötet, 1863, pp. 64. ( teljes szöveg [ Wikiforrás ]).
web Linkek
Egyéni bizonyíték
- ↑ Bejegyzés anilinre. In: Römpp Online . Georg Thieme Verlag, hozzáférés: 2017. május 19.
- ↑ a b c d e f g h i j Entry szóló anilin a GESTIS anyag adatbázisa az IFA , hozzáférhető a február 1, 2016. (JavaScript szükséges)
- ↑ David R. Lide (szerk.): CRC Handbook of Chemistry and Physics . 90. kiadás. (Internet verzió: 2010), CRC Press / Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, 3-26.
- ↑ bevitel anilin az osztályozási és címkézési jegyzékbe az az Európai Vegyianyag-ügynökség (ECHA), elérhető február 1-jén, 2016. A gyártók és a forgalmazók is bővíteni a harmonizált osztályozás és címkézés .
- ↑ Svájci Balesetbiztosítási Alap (Suva): Határértékek-jelenlegi MAK és BAT értékek ( 62-53-3 vagy anilin keresése ), hozzáférés: 2019. szeptember 14.
- ^ Hunnius Gyógyszerészeti szótár . 6. kiadás. Walter de Gruyter, Berlin / New York 1986, 68. o.
- ^ Henri A Favre, Warren H Powell: A szerves kémia nómenklatúrája: IUPAC ajánlások és preferált nevek 2013 . Szerk .: The Royal Society of Chemistry. Cambridge 2014, ISBN 978-0-85404-182-4 , pp. 416, 668 .
- ↑ Otto Unverdorben: A szerves testek viselkedéséről magasabb hőmérsékleten , Annalen der Physik und Chemie , 1826 , VIII , S. 397-410 ( korlátozott előnézet a Google könyvkeresőben).
- ↑ FF Runge: A szénpárlat egyes termékeiről , Annalen der Physik und Chemie , 1834 , XXXI , 65-78. O. ( Doi: 10.1002 / andp.18341070502 ; korlátozott előnézet a Google könyvkeresőben).
- ↑ J. Fritzsche: Az anilinről, az indigo új bomlástermékéről , Annalen der Chemie , 1840 , 36 (1), 84-90. O. ( Doi: 10.1002 / jlac.18400360108 ).
- ↑ Dr. N. Zinin: leírása néhány új szerves bázisok által képviselt a hidrogén-szulfid vegyületek szénhidrogének subnitric savval , Journal gyakorlati Chemistry , 1842 , pp. 140-153 ( doi: 10.1002 / prac.18420270125 ; korlátozott előnézet a Google Könyvkereső).
- ↑ AW Von Hofmann, JS Muspratt: Neue Bildungsweise des Anilins , Annalen der Chemie , 1845 , 53 (2), 221–229. Oldal ( doi: 10.1002 / jlac.18450530206 ; korlátozott előnézet a Google könyvkeresőben).
- ↑ AW von Hofmann: A benzolra adott biztonságos reakcióról , Liebigs Annalen , 1845 , 55 (2), 200–205. Oldal ( doi: 10.1002 / jlac.18450550205 ).
- ↑ In: Ber. dt. Chem. Ges. , 23, 1890, 3043, gallica.bnf.fr
- ↑ H. Wittcoff et al.: Industrial Organic Chemicals . 2004, 7. fejezet, 294. o.
- ↑ March, Jerry, 1929-1997.: March fejlett szerves kémiája: reakciók, mechanizmusok és szerkezet. 6. kiadás. Wiley-Interscience, Hoboken, NJ 2007, ISBN 0-471-72091-7 (angol).
- ↑ E. Gelpi és mtsai: A spanyol mérgező olaj szindróma 20 évvel a kezdete után: A tudományos ismeretek multidiszciplináris áttekintése . In: Environmental Health Perspectives , 2002, 110 (5), 457-464 , PMID 12003748 ; PMC 1240833 (ingyenes teljes szöveg).