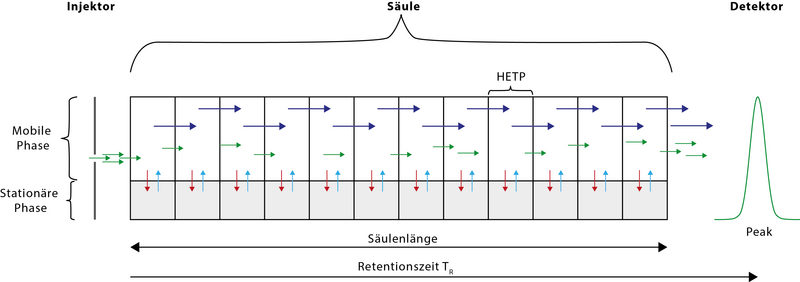
Gáz kromatográfia
A gáz-folyadék-kromatográfia (GLC) vagy egyszerűen a gáz-kromatográfia (GC) mind adszorpció, mind pedig megoszlás , analitikai módszerként széles körű a keverékek elválasztására az egyes alkalmazott vegyületekké. A GC csak olyan komponensekhez használható, amelyek gáz formában vagy bomlás nélkül elpárologhatnak (forrásponttartomány 400 ° C-ig). Az ilyen típusú kromatográfiában inert gázt , például nitrogént vagy héliumot használnak mozgófázisként , különleges esetekben pedig hidrogént . A vivőgázt egy tekercselt, ívelt, kapillárisszerű csövön , az úgynevezett oszlopon keresztül préselik , amely általában 10-200 méter hosszú.
Ez az elválasztó oszlop vagy fémből készül (régebbi modellekben), de ma főleg kvarcüvegből készül , amelyet bevonattal látnak el a törésállóság növelése érdekében. Belül egy meghatározott állófázissal van kibélelve (gyakran viszkózus poliorganosiloxánokkal ), és hőmérséklet-szabályozott kemencében helyezkedik el.
Miután bejutott egy minta anyagba, amelyet a vivőgáz szállít, az alkatrészek az oszlop álló fázisán különböző ideig maradnak , az egyes gázmolekulák polaritásától és gőznyomásától függően . Egy detektor méri a kilépés idejét az oszlop végén; Az érzékelőhöz rögzített felvevővel ez az időpont és az anyag mennyisége grafikusan megjeleníthető és összehasonlítható a szokásos anyagokkal. Ez lehetővé teszi az anyagok nagyon összetett keverékeinek nagyon gyors és egyszerű minőségi és mennyiségi meghatározását. A nagy teljesítményű folyadékkromatográfiával (HPLC) ellentétben csak kellően illékony anyagok detektálhatók.
Technológia története

A gázkromatográfia fejlődését Archer JP Martin , Erika Cremer és Fritz Prior alapvető munkája alakította ki . A történelem első gázkromatogramját röviddel a második világháború után hozták létre, és Cremeer Erika laboratóriumából származik. Megmutatja a levegő és a szén-dioxid elválasztását az aktív szénen. 1951-ben Anthony Trafford James és Archer JP Martin fejlesztették ki a jelenlegi értelemben vett első gázkromatográfot . Első, 1952-ben megjelent munkája a karbonsavak GC-elválasztását mutatta be. James E. Lovelock 1957-ben kifejlesztett elektronfogó detektorát (ECD) lehetővé tette a klórozott környezeti toxinok, például a PCB és a klórozott peszticidek, például a DDT érzékeny detektálását a GC által. Az ezt követő években számos olyan cég jelent meg, amelyek kereskedelmi gázkromatográfokat kínáltak, mint például a Pennsylvaniai Avondale-i F&M Scientific Corporation , amelyet a Hewlett-Packard vett át 1965 - ben . A kapilláris gázkromatográfia kifejlesztése az 1970-es években következett, mérföldkőnek számított Raymond D. Dandenau és Ernest Zerrender "olvadt szilícium-dioxid-oszlop" találmánya. Az első gyakorlati kapcsolatok a kapilláris gázkromatográfia és a tömegspektrometria (GC-MS) között nem sokkal később következtek . Ma a gázkromatográfia az egyik legfontosabb elemzési technika a vegyi laboratóriumokban.
Mérési elv
Az anyagok keverékének kromatográfiás elválasztása a gázkromatográfban a legegyszerűbb esetben egy nem poláros hordozóoszloppal történik, kizárólag a keverékben lévő egyes anyagok különböző forráspontjai alapján, így nincs különösebb kölcsönhatás a vegyülettel. állófázis, de "csak" tízezerszer ismételt adszorpció és deszorpció . Poláros elválasztó oszlopok esetén azonban a hasonló paraffinokkal megegyező forráspontú alkoholok, észterek, ketonok erősebben megmaradnak. A speciális kölcsönhatás - pontosabban a gázfázis és az állófázis közötti egyensúly - Raoult-törvény néven ismert . Raoult törvénye szerint minél nagyobb az anyag parciális gőznyomása, azaz Vagyis minél hosszabb az anyag a gázfázisban, annál rövidebb a retenciós idő .
A minta komponensei és az állófázis közötti kölcsönhatások erősségét mind szerkezetük, mind funkcionális csoportjaik határozzák meg. Nem poláros anyagok esetében csak a diszperziós kölcsönhatások ( van der Waals-kötések ) fordulnak elő, míg a poláris elválasztási fázisok szintén poláris kölcsönhatásba léphetnek, pl. B. hidrogénkötések vagy donor-akceptor kötések. Utóbbiak az elv szerint válnak szembe: az ellentétek vonzanak. Ez azt jelenti, hogy az elválasztási fázisok, amelyek z. B. képesek hidrogént felvenni a hidrogénkötésre, képesek szétválasztani azokat az anyagokat, amelyek hidrogént biztosíthatnak a kötéshez (pl. Alkoholok). Például az enantiomerek , amelyek forráspontjaikban nem különböznek egymástól, és ezért azonos a retenciós idejük, különféle erősségű kölcsönhatásokkal különválaszthatók a ciklodextrinek speciális származékaival is .
A gázkromatográfia alapkövetelménye, hogy a megvizsgálni kívánt anyag elpárologhasson bomlás nélkül - feltéve, hogy még nem gáznemű. Révén származékképzés , analitok, amelyek egyébként nehezen megközelíthető, mint például alkoholok, aminok, zsírsavak vagy cukrok, lehet termikusan stabilizált, hogy olyan mértékben, hogy ezek elválaszthatók a kereskedelmi forgalomban kapható fázisokat nehézség nélkül. Lehetséges származékokat karbonsavak a metil-észterek (átalakítás BF 3 és MeOH), az alkoholok a szilil-éterek .
A készülék fontos részei
A gázkromatográf három fő komponensből áll: injektor, elválasztó oszlop a GC kemencében és detektor. Az injektorban az alacsony forráspontú oldószerben oldott mintát egy lyukasztó membránon (szeptumon) keresztül injektáljuk. Ezt az injektort általában melegítik (450 ° C-ig) a minta gyors és teljes párolgása érdekében. Szeptummentes adagolás és lassú párologtatás hidegtápláló rendszerrel (KAS / PTV) is lehetséges. Az anyagokat a vivőgáz (az oszlop nyomása általában 6 bar-ig) az elválasztó oszlopba (kapilláris) szállítja, amelyet az úgynevezett GC kemencébe építenek. Ezt használják az elválasztó oszlop pontos temperálására annak érdekében, hogy az anyagok keverékét gyors és kiterjedt szétválasztás érje el állandó hőmérsékleten (izotermikus) vagy szabályozott hőmérséklet-emelés révén.
Az oszlop végén található egy detektor , amely elektronikus jelet generál, amikor egy anyag elhagyja a szeparációs rendszert. Az elektronikus jel csúcsként regisztrálható a felvevőn. A jeleket ezután egy integrátoron, vagy manapság leginkább a megfelelő kiértékelő szoftverrel ellátott számítógépes rendszeren dolgozzák fel. Az anyagkeverék elválasztásához és a különféle csúcsok kromatogramon való megjelenítéséhez szükséges idő gyakran 30 és 60 perc között van.
Injektorok
Az injektor segítségével a vizsgálandó anyagkeveréket felvesszük az elválasztó oszlopra. Általános injektorok / módszerek:
- Hasított / osztatlan injektorok ( SSL )
- Oszlopon lévő injekciók ( OCI ), közvetlen befecskendezéssel az oszlopra
- Hideg betápláló rendszerek (gyártótól, KAS-tól vagy PTV-től függően )
- Közvetlen betápláló rendszerek szelep áramkörök segítségével
Csomagolt oszlopok esetében az optimális minta mennyiség komponensenként 0,1 és 1 μl között van, kapilláris oszlopok esetében az optimális minta mennyiségének 100-1000-szer kisebbnek kell lennie. Speciális 1–10 μl-es fecskendők állnak rendelkezésre az oldószerrel is hígítható minta injektálására. Az injekció szempontjából fontos, hogy a fecskendőben ne legyen levegő (buborékok), mivel ez hozzájárulna a kemence kamrájában lévő anyagok oxidációjához.
Az úgynevezett autosmintákat , amelyek nagyszámú minta szekvenciális feldolgozását teszik lehetővé, gyakran használják osztott / osztatlan injektorokkal és hideg befecskendező rendszerekkel. Továbbá, is gőztérmintavevővel , kihajtás és befogás rendszerek és pyrolyzers használt minta-alkalmazás. Egy meglehetősen új fejlemény a szilárd fázisú mikroextrakció (SPME) vagy a keverőszáras szorbciós extrakció (SBSE) alkalmazása.
Használt oszlopok
Az elválasztó oszlopok fontos paraméterei:
- az oszlop átmérője
- az oszlop hossza
- és az állófázis típusa (foglaltság).
Korábban többnyire csomagolt oszlopokat használtak. A vékony (<1 cm) néhány méter hosszú fém- vagy üvegcsőben , az úgynevezett oszlopban szilárd, inert hordozóanyag található. Ha a vizsgálandó anyaggal rendelkező gázt közvetlenül a hordozóanyagon vezetik át, akkor GSC-nek ("Gas-Solid-Chromatography") nevezik. Ha a hordozóanyagot vékony, nagy molekulatömegű, viszkózus és nem túl illékony folyadékkal is bevonják, ez egy GLC ("Gas-Liquid-Chromatography"). Ez a folyadék itt veszi fel a tényleges állófázis funkcióját. Az itt alkalmazott inert gáz előnyösen nitrogén .
Az elmúlt évtizedekben túlnyomórészt a Marcel JE Golay által 1958-ban kifejlesztett kapilláris gázkromatográfiát használták . Előnye az anyagok kb. 100–1000-szer jobb elválasztása ( kb. 300 000 elválasztási szakasz száma ) a becsomagolt oszlopokhoz képest, így az elemzési idő is lerövidülhet. A stabilizálás érdekében a külső részén poliimiddel bevont kvarcüveg elválasztó oszlopok belső átmérője általában 0,1–0,5 mm, hossza pedig 10–60 m. A zsírsav-észterek elválasztására akár 100 m-ig kombinált oszlopokat is alkalmaznak. Az állófázis a kapillárisot csak vékony filmként vonja be, általában 0,1-5 µm. Az előny a hasonló anyagok drasztikusan jobb elválasztása a töltött oszlopokhoz képest. A GC trendje jelenleg egyre vékonyabb és rövidebb oszlopok felé mutat, mert ez jelentősen lerövidítheti az elemzésekhez szükséges időt. Az inert gáz előnyösen hélium , de hidrogént vagy ritkábban nitrogént is használnak.
Az állófázis osztályozásának fontos kritériuma a foglaltság polaritása . A nem poláros oszlopokon (DB-1 vagy hasonló típusú) lévő analitok általában forráspontjuk szerint eluálódnak. A poláris vegyületek viszont szelektíven lépnek kölcsönhatásba a poláros oszlopokban lévő poláris állófázisokkal, és polaritásuktól függően hosszabb ideig maradnak fenn, és később eluálódnak, mint az összehasonlítható nem poláros vegyületek, például B. alkánok . Különböző gyártók oszlopainak használatakor meg kell jegyezni, hogy az azonos helyhez kötött elválasztási fázisok sokféle nevet kapnak. A közös helyhez kötött elválasztási fázisok alábbi felsorolása megmutatja, hogy a különböző gyártók elválasztó oszlopai összehasonlíthatók-e az elválasztó oszlopok foglaltságának összetétele szempontjából.
| Az elválasztó oszlop foglaltságának összetétele |
Gyártó megnevezése | Hőmérsékleti tartomány | polaritás |
|---|---|---|---|
|
100% -os polidimetil-sziloxán |
DB-1, SB-1, BP-1, CP-Sil 5 CB, OV-1, OV-101, PB-1, SPB-1, RTX-1, PE-1, Ultra 1, ZB-1, AT -1, SE-30 | -50 ° C és +350 ° C között | nem poláris |
|
Polifenil- metil- sziloxán 5% fenil, 95% dimetil |
DB-5, SB-5, BP-5, CP-Sil 8 CB, PVMS-5, PB-2, SPB-5, Rtx-5, PE-2, Ultra 2, ZB-5, AT-5, SE -54, Optima-5, RSL-200 | -20 ° C és +350 ° C között | enyhén sarkos |
|
Polifenil- metil- sziloxán 14% fenil, 86% dimetil |
DB-624, SB-624, CP-Sil 13 CB, VOCOL, Rtx-Volatiles, PE-502, AT-62 | ± 0 ° C és +250 ° C között | közepes sarki |
|
Poli- ciano-propil-fenil-metil- sziloxán 6% ciano-propil-fenil, 94% dimetil |
DB-1301, SB-1301, Rtx-1301, AT-1301 | ± 0 ° C és +230 ° C között | poláris |
|
Polifenil- metil-ciano- sziloxán 6% fenil, 6% ciano, 88% metil |
DB-1701, SB-1701, BP-10, CP-Sil 19 CB, PB-1701, SPB-7, Rtx-1701, PE-1701, PAS-1701, AT-1701, RSL-300 | -50 ° C és +225 ° C között | poláris |
| Polietilén glikol | DB-WAX, SB-Wax, BP-20, CP-Wax 52 CB, Supelcowax-10, Stabilwax, PE-CW, HP-20M, AT-Wax | ± 0 ° C és +220 ° C között | poláris |
| Polietilénglikol-2-nitro-tereftálsav-észter | OPTIMA FFAP, DB-FFAP, HP-FFAP, CP-Sil 58 CB, 007-FFAP, CP-FFAP, Nukol | ± 0 ° C és +250/260 ° C között | poláris |
Az 1990-es évek eleje óta az oszlopgyártók nagy erőfeszítéseket tettek az alacsony vérzésű oszlopok kifejlesztésére, amelyeket elsősorban a GC-MS-ben használnak . Ezeket gyakran a "-ms" további megnevezéssel lehet felismerni.
A királis állófázissal borított elválasztó oszlopok felhasználhatók az enantiomer elemzésére. Ez lehetővé teszi az enantiomer arány meghatározását enantiomer keverékekben és az állítólag tiszta enantiomerek enantiomer tisztaságának elemzését .
Detektorok
A következő detektorokat használják:
- A lángionizációs detektor (FID), általában a szerves vegyületek számszerűsítésére, a legelterjedtebb detektor a gázkromatográfiában
- Hővezető detektor (TCD vagy TCD) tartós gázokhoz
- Photoionization Detector (PID)
- Lángfotometrikus detektor (FPD), elemspecifikus
- Nitrogén-foszfor detektor (angol NPD, szintén termionos detektor , TID), nitrogén-foszfor-specifikus
- Elektronfogó detektor (ECD) halogénezett szerves vegyületekhez
- Impulzus töltésérzékelő (PD), halogénezett szerves vegyületekhez is
- Atomkibocsátás-érzékelő (AED), elemspecifikus
- Echelle plazmaemisszió detektor (EPED), elemspecifikus
- Tömegspektrométer , tömegszelektív detektor (MS vagy MSD)
- Illékony szerves vegyületek ionmozgási spektrométere (IMS)
- Szagérzékelő (emberi orr)
Előfordul, hogy két (vagy több) detektor sorba van kapcsolva speciális kérdésekhez (tandem elv). Ennek alapkövetelménye azonban az, hogy az elülső detektorok ne hajtsák végre romboló módon a mérést (pl. ECD / TLD, de ne FID / NPD).
A detektor elektronikus jeleit 2D-s grafikonként, az úgynevezett kromatogramként jelenítik meg, az injektálás óta eltelt idő (retenciós idő) függvényében . Ez általában elektronikus kiértékelő egységek (kromatográfiai adatrendszerrel rendelkező számítógépek) segítségével történik, ritkán csak plotterekkel.
Alkalmazás az analitikában
A gázkromatográfia nagyon érzékeny módszer az anyagok keverékeinek elemzésére. Még minimális mennyiségű anyag ( 10–9 gramm) is kimutatható. Használható az összetett anyagkeverékek különálló komponensekre történő szétválasztására. Sok esetben önmagában a retenciós idő elegendő ahhoz, hogy az anyagot azonosítani lehessen az idő alatt, amely egy anyagnak az injekció beadásától a detektoron való áthaladásáig tart . Tömegspektrométerrel , az úgynevezett GC / MS kapcsolással kombinálva nagyon kis mennyiségű anyag detektálható és a szerkezet felderítése egyszerre végezhető el.
A gázkromatográfiát használják a herbicidek , a húskészítmények hormonok mezőgazdasági termékeinek elemzésére , a gyógyszerek , aromák és illóolajok, szénhidrátok , ásványolaj-összetevők és az igazságügyi kémia vizsgálatára, doppingvizsgálatokban, levegő- és tengervízvizsgálatokban a környezeti elemzések során . A hőmérsékleten stabil álló szilikon fázisokban még a nagy molekulájú anyagok is elválaszthatók, azonosíthatók és mennyiségileg meghatározhatók , például trigliceridek és viaszok . A nehezen illékony analitokat az elemzés előtt esetleg derivatizálni kell, azaz illékonyabb anyagokká kell átalakítani. Ez pl. B. trimetil-szulfónium-hidroxiddal vagy klór- trimetil- szilánnal végezzük a poláros csoportok nem-poláris metilezett csoportokká alakításával.
Használat a kvantitatív elemzésben
A detektor által megjelenített felületi egységek mérete ritkán kapcsolódik közvetlenül az elemzendő minta tényleges tömegfrakcióihoz. Ez teszi kalibráció a referencia anyag egy meghatározott tartalom szükséges. A gázkromatográf (különösen a befecskendező rendszer ) hibáinak kizárása érdekében gyakran használnak belső standardokat , különösen a gázkromatográfiában . Belső standardként egy további anyag szolgál itt, amelynek retenciós ideje közel áll a meghatározandó analithoz, de nem helyezi el egymással. Hozzáadják az analithoz és a referencia anyaghoz vagy az abból készített oldatokhoz. A mérés után meghatározzuk az analit és a referenciaanyag megfelelő csúcsterületeit a belső standard csúcsterületéhez viszonyítva, és a lehető legnagyobb mértékben kiszámoljuk az injekciós rendszer hibáit. Kalibrálás után a P minta cP koncentrációja meghatározható az alábbi egyenlet segítségével.
c S a standard kimért koncentrációja, A a kromatogram csúcsának területét és r az anyag érzékenységét jelöli (mennyi jelet mutat a detektor M-enként). r egy adott detektorhoz egyszer mérhető, majd táblázatos.
irodalom
- Ernst Bartholomé et al. (Szerk.): Ullmanns Encyklopadie der technischen Chemie . 5. kötet: Hans Kelker (Szerk.): Elemzési és mérési módszerek. 4., átdolgozott és kibővített kiadás. Verlag Chemie, Weinheim és munkatársai, 1980, ISBN 3-527-20005-3 , 118. o.
- Eberhardt Leibnitz, Hans Georg Struppe (szerk.): A gázkromatográfia kézikönyve. 3., átdolgozott és nagymértékben kibővített kiadás. Geest & Portig KG akadémiai kiadóvállalat, Lipcse, 1984, ISBN 3-89141-001-8 .
- Gerhard Schomburg : gázkromatográfia. Alapok, gyakorlat, kapilláris technológia. 2., átdolgozott és kibővített kiadás. VCH, Weinheim és mtsai., ISBN 3-527-26461-2 .
- Reiner Wittkowski , Reinhard Matissek (Szerk.): Kapilláris gázkromatográfia az élelmiszer-ellenőrzés és kutatás területén , B. Behr's Verlag GmbH & Co., Hamburg 1992, ISBN 3-86022-037-3 .
- Peter J. Baugh (Szerk.): Gázkromatográfia. Felhasználó-orientált prezentáció. Vieweg, Braunschweig et al., 1997, ISBN 3-540-67009-2 .
- Walter David, Burkhard Kusserow: GC tippek. Problémamegoldások a gázkromatográf körül. Hoppenstedt, Darmstadt 1999, ISBN 3-8203-0469-X .
- Bruno Kolb: Gázkromatográfia képekben. Wiley-VCH, Weinheim és munkatársai, 1999, ISBN 3-527-29880-0 .
- Keith D. Bartle, Peter Myers: A gázkromatográfia története. In: Az analitikai kémia tendenciái . Vol. 21, No. 9/10, 2002. szeptember 10., 547-557. Oldal, doi : 10.1016 / S0165-9936 (02) 00806-3 .
web Linkek
- ETH Zürich, analitikai kémia: gázkromatográfia (GC) (PDF; 991 kB)
- Szimuláció valósul meg a NetLogo-ban .
Egyéni bizonyíték
- ↑ lásd: LC GC International , 3. évf. 11.
- ↑ AT James, AJP Martin: Gáz-folyadék megoszlási kromatográfia: az illékony zsírsavak elválasztása és mikro-becslése hangyasavból dodekánsavvá . In: Biokémiai Közlöny . 50, 1952, 679-690.
- ^ JE Lovelock: Érzékeny detektor gázkromatográfiához . In: Journal of Chroma . 1. szám, 1958., 35–46. doi : 10.1016 / S0021-9673 (00) 93398-3 .
- ^ JE Lovelock: Az elektron befogó detektor . In: Journal of Chroma . 99, 1. szám, 1974., 3–12. doi : 10.1016 / S0021-9673 (00) 90840-9 .
- ^ Dandenau, Raymond D. és EH Zerenner: A szemüveg vizsgálata a kapilláris kromatográfiához . In: Journal of High Resolution Chromatography . 2, 6. szám, 1979., 351-356. doi : 10.1002 / jhrc.1240020617 .
- ↑ Infographic - Az analitikai kémia hihetetlen fejlődése. In: Német festékintézet. Letöltve: 2019. augusztus 10 .
- ↑ Dioxin elemzés. In: Szövetségi Kockázatértékelési Intézet. Letöltve: 2019. augusztus 10 .
- ↑ Wolfgang Brodacz, Marc Platthaus: GC fázisok összehasonlítása és kombinációja. LaborPraxis, 4/2004.
- ↑ N. Limsathayourat, H.-U. Melchert: Szénhidrogének, zsírsavszármazékok, koleszterin-észterek, viasz-észterek és trigliceridek magas hőmérsékletű kapilláris GLC-je a méhviasz elemzésében. In: Fresenius 'Journal of Analytical Chemistry. 318, 6. szám, 1984, 410-413 . Oldal, doi : 10.1007 / BF00533223 .
- ↑ Uri Wilensky : NetLogo Models Library: Gázkromatográfia. Hozzáférés: 2018. november 27 .