Kálium-karbonát
| Szerkezeti képlet | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
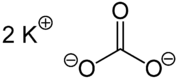
| ||||||||||||||||||||||
| Tábornok | ||||||||||||||||||||||
| Vezetéknév | Kálium-karbonát | |||||||||||||||||||||
| más nevek | ||||||||||||||||||||||
| Molekulaképlet | K 2 CO 3 | |||||||||||||||||||||
| Rövid leírás |
fehér szilárd anyag |
|||||||||||||||||||||
| Külső azonosítók / adatbázisok | ||||||||||||||||||||||
| ||||||||||||||||||||||
| tulajdonságait | ||||||||||||||||||||||
| Moláris tömeg | 138,20 g mol -1 | |||||||||||||||||||||
| Fizikai állapot |
határozottan |
|||||||||||||||||||||
| sűrűség |
2,428 g cm -3 |
|||||||||||||||||||||
| Olvadáspont |
891 ° C |
|||||||||||||||||||||
| forráspont |
bomlás |
|||||||||||||||||||||
| oldhatóság |
nagyon könnyű vízben (1120 g l- 1 20 ° C-on) |
|||||||||||||||||||||
| biztonsági utasítások | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikológiai adatok | ||||||||||||||||||||||
| Termodinamikai tulajdonságok | ||||||||||||||||||||||
| ΔH f 0 |
−1151,0 kJ / mol |
|||||||||||||||||||||
| Lehetőség szerint és szokás szerint SI egységeket használnak. Eltérő rendelkezés hiányában a megadott adatok a standard feltételekre vonatkoznak . | ||||||||||||||||||||||
Kálium-karbonátot (műszaki nyelv), vagy kálium-karbonát (közös név : hamuzsír ), K 2 CO 3 , egy alkálifém , és a kálium- sója szénsav . Fehér, higroszkópos port képez , amelynek olvadáspontja 891 ° C és sűrűsége 2,428 g · cm −3 . A hamuzsír elnevezés abból a régi módszerből származik, hogy a növényi hamu (különösen a fahamu , de a tengeri moszat hamu ) kálium-karbonátjának dúsítását úgy végezzük, hogy vízzel kimossuk (innen ered a "lúgos só" elnevezés), majd cserépben bepároljuk. A hagyományos név inspirálta az angol kálium és kálium elnevezéseket is , amelyek szerint a kálium sok ásványi káliumsót tartalmaz (pl. Kálium-klorid ), és jobb kálium- sóként lefordítani.
Esemény
A világ legnagyobb kálium-só betétek vannak Kanadában , Oroszországban , Eritrea , Fehéroroszország és Németország ; A kálium-karbonát néhány belvízben is megtalálható, például a Holt-tengerben vagy a Lop Nor-sivatagban . Korábban a káliumot fahamuból nyerték ki kimosással . Az ásványi anyagok fahamu tartalma körülbelül 85%; ennek körülbelül 14-19% -a kálium-karbonát és nátrium-karbonát.
Kivonás és bemutatás
- Kálium-hidroxid karbonizálása :
- A felhasznált CO 2 fő forrása az égési gázok.
- A mésztej ( kalcium-hidroxid- oldat) reakciója kálium-szulfáttal és szén-monoxiddal 30 bar nyomáson (formiát-eljárás). Az elválasztott kálium-formiátot ezután oxidatív módon kalcinálják:
- Kimosódás növényi hamu és az azt követő lepárlással hamu házak (már nem történelmileg vagy technikailag fontos)
- történeti: fogkőégetés (a Tartarus calcinatus égetett fogkő), például Paracelsusban
A nátrium- karbonáthoz hasonlóan a kálium-karbonát sem nyerhető az ammónia-szóda eljárással, mivel a kálium-hidrogén-karbonát (KHCO 3 ) köztitermék túl oldható.
tulajdonságait
A víz , ez nagyon könnyen és könnyen oldódó (1120 g / l), miáltal a hő szabadul. Az oldat hidroxid-ionok képződésével reagál lúgosra :
- A karbonátion vízzel reagálva hidrogén-karbonát-iont és hidroxid-iont képez.
Savakkal a megfelelő kálium-sók képződnek a szén-dioxid fejlődésével. Szobahőmérsékleten dihidrátként kristályosodik a vizes oldatból.
Vízmentes kálium-karbonátot kristályosodik monoklinként , tércsoport P 2 1 / c (tércsoport nélkül. 14) a rácsparamétereket egy = 5,640 Á , b = 9,839 Á, c = 6,874 Á és β = 98.70 °. 250 ° C-on ezt a változások a monoklin β-formában (tércsoport C 2 / C (No. 15) , egy = 5,675 Á, b = 9,920 Á, c = 7,018 Á és β = 96,8 °). 450 ° C-on ez hatszög alakúra változik .
használat
- Adalékanyag az üveg gyártásában
- Puha szappanok gyártása
- Káliumüveg gyártása
- Festékek gyártása
- Fényképészeti fejlesztők gyártása
- Műtrágyák gyártása (káliumellátó komponens)
- Vízmentes kálium-karbonátot alkalmanként szárítószerként használnak a laboratóriumban .
- Növénynövelő szer lapos pékárukhoz ( sütik és mézeskalács , főleg karácsonyi pékség ) és magas cukortartalmú tésztákhoz.
- Adalékanyag a kakaóhoz, mint savasságszabályozó
- Semlegesítő szer, ha sósavat (E 507) használnak aroma fokozóként .
- A mazsola gyors száradása: A szőlő természetes viaszrétegének eltávolításával a nedvesség könnyebben elpárolog.
- Alaptermék más káliumvegyületekhez.
- A kéreg eltávolítása a fazekakból: 1 evőkanálnyit tegyen az edénybe a kéregre, hagyja egy éjszakán át állni, és másnap forraljon fel egy csésze vízzel; a maradványok pelyhesen lazulnak ki az edény aljáról.
- Formaleválasztó gipszkötés ( szobor )
- Elektrolit komponens olvadt karbonát üzemanyagcellákban
- Dohány-adalék a tubákhoz (Németországban a dohányrendelet szerint )
- Adalékanyag bizonyos függőséget okozó anyagok beviteléhez
- Adalék néhány kézmosó folyékony szappanban
- Környezetbarát jégmentesítő ( jégtelenítő só helyett ) a fekete jéghez az utcákon és a járdákon
- Mivel mindig tartalmaz radioaktív kálium-40-et, a kálium felhasználható a radioaktivitással kapcsolatos hallgatói kísérletekhez
- Sok évszázados Európában, kálium-karbonát formájában bükk kőris használták a hasa ruházati és egyéb textíliák készült ágynemű és később is a pamut . A hamut zsákokba tesszük, és egy fahordóhoz adjuk, amely réteg mosoda van megtöltve. Azzal, hogy forró vizet önt a tasakra, lúg szabadult fel, amelynek tisztító és enyhén fehérítő hatása volt. A lúgot ezután vízzel mosták ki a mosókútnál vagy a folyónál. Az advent a túró szappan és újabb mesterséges tisztítószerek elején a 20. század ez a módszer elavult.
- Tűzoltószerek része
Szóda-kálium emésztés
A szóda- kálium emésztést rosszul oldódó (alkáliföldfém) szulfátokhoz, erősen lágyított (savas vagy amfoter) oxidokhoz, szilikátokhoz és ezüst-halogenidekhez használják; az emésztés Na 2 CO 3 / K 2 CO 3 olvadékban történik. A ZrO 2 , Zr 3 (PO 4 ) 4 , Al 2 O 3 , Cr 2 O 3 és Fe 2 O 3 csak részben oldódnak fel. Szódabikarbóna és hamuzsír keverékét használjuk erre az olvadék emésztésre, mert ez csökkenti az olvadáspontot a tiszta sókhoz képest ( eutektikus keverék ). Ezenkívül a karbonát óriási feleslege a termék egyensúlyára taszítja a reakció egyensúlyát.
Példa a szulfátokra:
Egyéni bizonyíték
- ↑ E 501 bejegyzés : Kálium-karbonát az élelmiszer-adalékanyagok európai adatbázisában, hozzáférés 2020. július 1-jén.
- ↑ bevitel kálium-karbonát , a CosIng adatbázisa az Európai Bizottság, elérhető augusztus 11-én, 2020-ra.
- ↑ a b c d e f g A kálium-karbonátra vonatkozó bejegyzés az IFA GESTIS anyagadatbázisában , elérhető 2017. február 22-én. (JavaScript szükséges)
- ↑ bevitel kálium-karbonátot a ChemIDplus adatbázisában United States National Library of Medicine (NLM)
- ↑ David R. Lide (Szerk.): CRC kémiai és fizikai kézikönyv . 90. kiadás. (Internetes változat: 2010), CRC Press / Taylor és Francis, Boca Raton, FL, Vegyi anyagok standard termodinamikai tulajdonságai, 5-20.
- ^ USGS (amerikai ásványi erőforrások programja): hamuzsír. (PDF; 88 kB) 2010. januárjától.
- ↑ Fahamu bejegyzés . In: Kémiai lexikon. Spektrum der Wissenschaft Verlagsgesellschaft, elérhető 2018. szeptember 3-án .
- ↑ Kálium-karbonát bejegyzés . In: Römpp Online . Georg Thieme Verlag, hozzáférés: 2014. november 12.
- ↑ Friedrich Dobler: Az orvostudomány kémiai alapjai, Theophrastus Paracelsus: Antimonkészítményeinek kísérleti áttekintése. In: A Nemzetközi Gyógyszerésztörténeti Társaság kiadványai , Új sorozat, 1957. 10., 76–86., Itt: 80. oldal.
- ^ Friedrich Dobler: Conrad Gessner mint gyógyszerész. Von Ostheim AG, Zürich 195, 104. o.
- ↑ Y. Idemoto, JW Richardson, N. Koura, S. Kohara, CK Loong: A (Li x K 1-x ) 2 CO 3 (x = 0,0,43,0,5,0,62,1) kristályszerkezete neutronpor-diffrakcióval elemzés. In: Journal of Physics and Chemistry of Solids, 59, 1998, p. 363-376, doi: 10.1016 / S0022-3697 (97) 00209-6 .
- ↑ HY Becht, B. Struikmans: A monoklinika magas hőmérsékletű módosítása a kálium-karbonátból. In: Acta Crystallographica , B32, 1976, 3344-3346, doi: 10.1107 / S0567740876010303 .
- ^ SJ Schneider, EM Levin: A K 2 CO 3 polimorfizmusa . In: Journal of the American Ceramic Society , 56 (4), 1973, 218–219. Oldal, doi: 10.1111 / j.1151-2916.1973.tb12461.x .
- ↑ A bécsi Természettudományi és Élettudományi Egyetem tanulmánya a nitrogéntartalmú olvasztószerek hatásairól Felolvasztó szerek vizsgálata 2000 (PDF; 1,6 MB)
- ↑ LVR Regionális és Regionális Történeti Intézet: Bükk hamu mosása
- ↑ Georg Pleß: Bizonyos, környezetre káros tűzoltószerek cseréje a kiválasztott alkalmazási területeken . Szerk .: Szász-Anhalt Tűzoltóság Intézete. Heyrothsberge 2003 ( Umweltbundesamt.de [PDF]).
web Linkek
- Stephanie Summermatter: Kálium. In: Svájc Történelmi Lexikona .







