amalgám
Egy amalgám ( ógörög μαλακός malakos „puha” a alfa privativum , azaz a „nem-lágyító”; szerinti másik etimológiai arab al malagma „bőrpuhító kenőcs”, vagy al-magam görög málagma ) van egy ötvözet a higany a kémiában . A tágabb értelemben vett amalgám gyakran más anyagok nem reverzibilis keveréke is, általában több fém ötvözete. Átvitt értelemben az amalgám különböző kifejezések, ötletek, kultúrák vagy hagyományok keveréke is.
Mivel sok fém oldódik a higanyban, nagyon sok amalgám van. Egyes fémek, például a vas , nem amalgámképzők. A magas higanytartalmú amalgámák szobahőmérsékleten gyakran folyékonyak, mint maga a higany; ha alacsonyabb a higanytartalom, akkor szilárdak.
A klasszikus alkímia esetében a higany más fémekkel való egyesítését ("koagulálását") gyakran összehasonlítják a fizikai egyesüléssel. Mivel alkímiai lexéma van a középkori latin amalgama elfoglalt a 13. század óta.
Természetes amalgámok

Számos természetesen előforduló amalgámot ismer és ismer el a Nemzetközi Ásványtani Szövetség önálló ásványként :
- Ólommal: ólom-amalgám (Pb 2 Hg)
- Rézzel : Belendorffit (Cu 7 Hg 6 ), Kolymite (Cu 7 Hg 6 )
- Palládiummal: Potarit (PdHg)
- Ezüsttel : eugenit (Ag 11 Hg 2 ), luanheit (Ag 3 Hg), moschellandsbergite (Ag 2 Hg 3 ), paraschachnerite (Ag 1,2 Hg 0,8 ), schachnerite (Ag 1,1 Hg 0,9 )
- Ezüsttel és arannyal: Weishanite ((Au, Ag) 3 Hg 2 )
Műszaki amalgámok és felhasználásuk
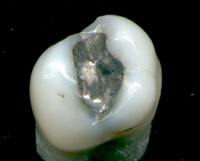
Fogászati amalgám
A fogászatban a higany ötvözetét más fémekkel, mint például ezüst, réz, indium, ón és cink, széles körben használják fogtöltő anyagként. A súlyos egészségügyi problémákkal való összefüggést nem sikerült bizonyítani. A higanynak minimálisan van kitéve.
Nátrium-amalgám
A szerves és szervetlen kémia és a nagy mennyiségben előállított amalgám technikailag fontos redukálószere a nátrium-amalgám , amely a klór-alkáli elektrolízis egyik változatának közbenső terméke. Vízzel bomlik le , így nátron , hidrogén és higany képződik , amelyet az áramkörben újra felhasználnak elektrolízishez .
Ammónium-amalgám
Mivel az alkálifémek amalgámokat képeznek, például az alkálifém-ionok higanyelektródos oldatainak elektrolízise során, kísérleteket tettek ammónium- vagy ammónia-amalgám előállítására is (az ammóniumion gyakran hasonlóan viselkedik, mint az alkálifémionoké); Az ammónium-amalgám azonban higanyra, ammóniára és hidrogénre bomlik .
Arany amalgám
A higanyot néha még mindig használják a kézműves aranybányászatban . A megfelelő aranytartalmú alapanyagokat keverjük vagy gyúrjuk (összeolvasztjuk) a folyékony higanyval. Ez formák egy kezdetben folyékony amalgám az arany, amely jelen van a kis pelyhek vagy granulátumok, őrölt ásványi, pörkölt érc koncentrátumok vagy laza üledékek szappan lerakódások , amely könnyen elválik a könnyebb összetevők miatt a nagyobb sűrűségű. Annak érdekében, hogy tiszta aranyat kapjon belőle, az amalgámot felmelegítik, amellyel a higany elpárolog; ezt a folyamatot dohányzásnak is nevezik. Higanygőzök keletkeznek, amelyek rendkívül veszélyesek az egészségre.
Az arany amalgámokat kémiai aranyozásban is használják, más néven tűz aranyozásként . Az arany amalgámot egy fémtárgyra viszik fel vagy festik, és a higany hő hatására elpárolog.
Alumínium-amalgám
Redukálószerként alumínium-amalgámot használnak.
Tallium amalgám
A tallium- amalgám olvadáspontja alacsonyabb, -58 ° C, mint a tiszta higanyé (-38,83 ° C), ezért - magas toxicitása ellenére - hőmérő folyadékként használják alacsony hőmérsékletű hőmérőkhöz .
Cink-amalgám
A cink-amalgámot redukálószerként használják a szerves szintetikus kémiában, különösen a Clemmensen-redukcióban az aldehidek vagy ketonok savas oldatban történő redukciójára . A szervetlen vagy analitikai kémiában a cink-amalgámot használták és használják viszonylag erős redukálószerként, pl. B. uranilsók vagy titanilsók redukciójához, kevésbé bázikus fémek amalgámjainak előállításához sóikból, pl. B. réz, nikkel vagy kobalt-amalgám. A tiszta cinkkel vagy más cinkötvözetekkel ellentétben a cink-amalgám nem fejleszt hidrogént; ezenkívül a cink-amalgám savval történő kezeléssel oxidmentessé tehető. Korábban cink-amalgámot is használtak rézfúváshoz . Annak érdekében, hogy megvédje a cink elektródákat a galvánelemek a korróziótól a fejlesztési hidrogén, ők is ötvöződik.
Egyéb
Az ón- amalgám a 19. század közepéig képezte a tükrök fényvisszaverő bevonatát .
Az amalgám az energiatakarékos lámpákban az egyébként műszakilag szükséges folyékony higany helyettesítésére használható . Az amalgám alkalmazásával a fényáram nagyobb hőmérséklet-tartományban szinte állandó marad . Ez az előny különösen hatékony, ha zárt lámpatestekben, földgömbházakban és szabadban használják. Hátrány az alacsony kezdeti fényáram bekapcsolás után, mivel a higany csak magasabb hőmérsékleten párolog el az amalgámból.
Az amalgámképző elemek listája
Az elemeket itt felsoroljuk (fő és másodlagos) csoportok és a sorszámok szerint.
| H | Hé | |||||||||||||||||
| Li | Lenni | B. | C. | N | O | F. | Nem | |||||||||||
| N / A | Mg | Al | Si | P. | S. | Cl | Ar | |||||||||||
| K | Kb | Sc | Ti | V | Kr. | | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | Mint | Se | Br | Kr | |
| Rb | Sr | Y | Zr | Nb | Hétf | Tc | Ru | Rh | Pd | Ag | CD | Ban ben | Sn | Sb | Te | ÉN. | Xe | |
| Cs | Ba | La | * | HF | Ta | W. | újra | Os | Ir | Pt | Au | Ed | Tl | Pb | Kettős | Po | Nál nél | Marg |
| Fr. | Ra | Ac | ** | Rf | Db | Vminek | Melltartó | Hs | Mt | Ds | Rg | Cn | ||||||
| * | Ce | Pr | Nd | Délután | Sm | Eu | Gd | Tuberkulózis | Dy | Ho | Ő | Tm | Yb | Lu | ||||
| ** | Th | Pa | U | Np | Micimackó | A | Cm | Bk | Vö | Azt | Fm | Md | Nem | Lr | ||||
Amalgám minta
A higanyfémekkel és az amalgámmal ellentétben a higany sói vízben való oldhatóságuk miatt nagyon mérgezőek. Az úgynevezett amalgámminta detektálja: A salétromsavoldatot rézlemezre helyezzük - ezüstös, letörölhetetlen amalgámfolt marad:
- Redox-reakció : A higanykationok a rézet rézionokká és higannyá oxidálják.
A higany ötvözetet képez a rézlemezzel, a réz-amalgammal. Az ezüst sók hasonló foltokat képeznének; a keletkező ezüst azonban letörölhető. Így végső soron az ezüst-sók megkülönböztethetők a higany-sóktól.
Amalgám folyamat
A klór-alkáli elektrolízis során klór , nátronlúg és hidrogéngáz nagy mennyiségű előállításához a higanyt használják katódként az amalgám folyamatban, így a redukcióval sós vízből képződött nátrium amalgámként kerül lerakódásra. A nátrium-amalgám ezután az amalgámbontóhoz kerül, ahol vízzel reagálva sómentes nátrium-hidroxidot, hidrogéngázt és higanyot képez. Ennek az elektrolízis eljárásnak az az előnye, hogy nátrium-hidroxidot (nátronlúgot) tartalmaz nátrium-kloridtól mentesen, de ökológiailag kérdéses, mivel a higanymaradványokat el kell távolítani a termékekből (utótisztítás, méregtelenítés, pl. Aktív szénszűrőkkel).
Lásd még
irodalom
- Wolf-Dieter Müller-Jahncke : Amalgám az alkímia. In: Werner E. Gerabek , Bernhard D. Haage, Gundolf Keil , Wolfgang Wegner (szerk.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin / New York, 2005, ISBN 3-11-015714-4 , 49. o.
- Curt Gerhard Lorber: Amalgám a fogászatban. In: Werner E. Gerabek et al. (Szerk.): Encyclopedia Medical History. 2005, 49. o.
web Linkek
Egyéni bizonyíték
- ↑ Jörg Barke: A chymie nyelve: az 1574-1761 közötti időszak négy nyomtatványának példájával. (= Német nyelvészet. 111). Tübingen 1991, 357. o.
- ↑ Ásványi atlasz: Amalgám
- ↑ Hogyan kezelik a fogszuvasodást? In: fogyasztói tanácsadó központ . 2018. január 23, megtekintve 2020. szeptember 7 .
- ↑ Kevés bizonyíték áll rendelkezésre a higanytöltések és az emberi egészségügyi problémák összekapcsolására. (PDF; 25 kB). Az LSRO sajtóközleménye a tanulmányról
- ↑ Az amalgámból készült fogtömések ártalmatlanok. In: A világ. 2004. december 14.
- ↑ Történelmi tükrök. itt: spiegelart.de , hozzáférés : 2015. november 24.
- ↑ ABC Chemie, Brockhaus-Verlag Leipzig, 1965, NDK, "Amalgame" bejegyzés 60. o. És / vagy a megfelelő elemneveken
- ↑ Hollemann / Wiberg: Szervetlen kémia tankönyve, 90. kiadás, bejegyzések az egyes elemek tulajdonságairól